Assalammu‘alaikum wr. wb.
Hello gaes! Apakah kalian malas belajar Fisika? Dan jangan malas untuk mempelajari tentang Ilmu Sains. Kali ini kita berjumpa lagi di Kelas 12, dan saya akan membahas tentang Rangkaian Arus Bolak-Balik, Gelombang Elektromagnetik, Teori Relativitas Khusus, Sumber Energi, dan Struktur Atom untuk Materi Pelajaran Fisika.
RANGKAIAN ARUS BOLAK-BALIK
Sumber Materi : Ruangguru (Blog) dan Soalkimia.com (Contoh Soal)
Tahukah kamu generator pembangkit listrik merupakan salah satu aplikasi dari rangkaian Arus Bolak-balik? Ternyata Rangkaian Arus Bolak-balik terdiri dari beberapa jenis yaitu Rangkaian Resistor, Induktor, dan Kapasitor. Bagaimana keadaan rangkaian-rangkaian tersebut saat dialiri arus bolak-balik? Mari kita simak pembahasan berikut ini.
Arus Bolak-balik atau Altenating Current (AC) merupakan arus dan tegangan listrik yang besarnya berubah terhadap waktu dan mengalir dalam dua arah. Arus bolak-balik biasanya dimanfaatkan untuk peralatan elektronik. Sumber arus bolak-balik prinsip kerjanya yaitu terjadi perputaran kumparan dengan kecepatan sudut tertentu yang berada dalam medan magnetik. Jenis-jenis rangkaian dalam rangkaian AC adalah Rangkaian Resistor, Rangkaian Induktor, dan Rangkaian Kapasitor.
1. Rangkaian Resistor
Sebuah Resistor akan dialiri arus bolak-balik ketika dihubungkan dengan sumber tegangan bolak-balik. Rangkaian resistor dalam arus bolak-balik digunakan untuk menurunkan potensial listrik dalam rangkaian atau sebagai pembatas arus listrik yang masuk sehingga arus dan tegangan dalam rangkaian resistor mempunyai fase yang sama saat terhubung dengan sumber tegangan bolak-balik.
 |
| Rangkaian Resistor pada Arus Bolak-balik |
 |
| Grafik hubungan Tegangan dan Arus terhadap Waktu pada Resistor |
Berdasarkan Grafik terlihat bahwa Tegangan dan Arus berada pada keadaan sefase artinya mencapai nilai maksimum pada saat yang sama. Sebuah resistor dihubungkan dengan sumber tegangan bolak-balik, besarnya Tegangan pada Resistor sama dengan tegangan sumber. Di bawah ini merupakan rumus tegangan resistor dan arus yang mengalir melalui Resistor.
 |
| Sumber : Blog Ruangguru |
2. Rangkaian Induktor
Sebuah Induktor mempunyai hambatan yang disebut Reaktansi Induktif saat dihubungkan dengan sumber tegangan bolak-balik. Hambatan atau Reaktansi Induktif bergantung pada Frekuensi Sudut Arus dan Induktansi diri Induktor atau dapat dirumuskan sebagai  .
.
 |
| Rangkaian Induktor pada Arus Bolak-balik |
 |
| Grafik hubungan Tegangan dan Arus terhadap Waktu pada Induktor |
Berdasarkan Grafik terlihat bahwa besar tegangan pada induktor adalah nol saat arus Induktornya Maksimum, begitupun sebaliknya. Artinya Tegangan pada Induktor mencapai nilai maksimum lebih cepat serempat periode daripada saat arus mencapai maksimumnya. Rumus tegangan dan arus yang mengalir pada induktor seperti berikut :
 |
| Sumber : Blog Ruangguru |
3. Rangkaian Kapasitor
Sebuah Kapasitor memiliki karakteristik yang dapat menyimpan Energi dalam bentuk muatan Listrik ketika dihubungkan dengan sumber tegangan bolak-balik maupun tegangan searah. Kapasitor yang dialiri arus bolak-balik akan timbul resistansi semu atau biasa disebut dengan reaktansi kapasitif. Besar nilai reaktansi kapasitif bergantung pada besarnya Nilai Kapasitansi Kapasitor dan Frekuensi Sudut Arus atau dapat dirumuskan sebagai  .
.
 |
| Rangkaian Kapasitor pada Arus Bolak-balik |
 |
| Grafik hubungan Tegangan dan Arus terhadap Waktu pada Kapasitor |
Berdasarkan grafik terlihat bahwa arus pada kapasitor maksimum saat tegangan kapasitor bernilai nol, begitupun sebaliknya. Artinya, arus mencapai nilai maksimumnya seperempat periode lebih cepat daripada saat tegangan mencapai nilai maksimumnya. Rumus tegangan dan arus yang mengalir pada kapasitor seperti berikut :
 |
| Sumber : Blog Ruangguru |
CONTOH SOAL
1. Susunan Seri Hambatan 40 Ω dan Kapasitor dengan Reaktasi Kapasitif 30 Ω dihubungkan dengan sumber arus bolak-balik, Tegangan Efektif 220 V. Tegangan Efektif pada Resistor adalah…
Pembahasan :
2. Susunan Seri Hambatan 80 Ω dan kapasitor dengan reaktasi kapasitif 60 Ω dihubungkan dengan sumber arus bolak-balik, tegangan efektif 300 V. Tegangan efektif pada kapasitor adalah…
Pembahasan :
3. Suatu rangkaian R-L-C dipasang pada tegangan bolak-balik yang nilai efektifnya 100 V dan Frekuensi 60 Hz. Bila R = 10 Ω, L = 26,5 F, maka tegangan di ujung-ujung L adalah…. V
Pembahasan :
4. Sebuah sumber daya 200 V, 50 Hz dihubungkan dengan resistor murni 400 Ω dan sebuah kapasitor seri. Jika tegangan pada resistor itu 160 V. Tentukan tegangan pada kapasitor itu….
Pembahasan :
5. Sebuah sumber daya 130 V, 50 Hz dihubungkan dengan resistor murni 400 Ω dan sebuah kapasitor seri. Jika tegangan pada resistor itu 50 V. Tentukan reaktasi kapasitor itu….
Pembahasan :
6. Sebuah Resistor 20 Ω disusun seri dengan sebuah kapasitor. Rangkaian dihubungkan ke sebuah tegangan sumber yang frekuensinya dapat berubah-ubah. Jika tegangan antara ujung-ujung resistor sama dengan tegangan antara ujung-ujung kapasitor , tentukanlah frekuensi sumber AC tersebut!
Pembahasan :
7. Sebuah kumparan dengan hambatan listrik dapat diabaikan dihubungkan ke sebuah sumber AC 60 V, 400 Hz. Jika arus dalam kumparan adalah 1,2 A, maka induktasi kumparan adalah…
Pembahasan :
8. Perhatikan Rangkaian RLC berikut ini!
Tentukan nilai impedansi pada rangkaian diatas!
Pembahasan :
Diketahui :
V =120 V
ω = 400 rad /s
R = 200 Ω
L = 2,5 H
C = 4 μF
Ditanya : Z = … Ω ?
9. Perhatikan Rangkaian RLC dibawah ini!
Rangkaian seri RLC terdiri dari resistor, induktansi induktor, kapasitas kapasitor yang dihubungkan seri dengan tegangan 200 volt dan frekuensi anguler 500 rad/s. Jika impedansi dalam rangkaian 250 Ω, maka tentukan besar faktor daya pada rangkaian diatas!
Pembahasan :
Diketahui :
L = 800mH
C = 8mF
V = 200V
w = 500rad /s
Z = 250 Ω
Ditanya : ?
cos Θ …?
10. Suatu rangkaian seri RLC dihubungkan pada tegangan listrik bolak-balik dengan nilai Tegangan Efektif 120 Volt, arus efektif yang mengalir sebesar 12 A dan kecepatan sudut sebesar 125 rad/s. Apabila R = 8 Ω, L = 32mH, dan C = 800µF, maka tentukan besar daya yang dipakai dalam rangkaian!
Jawaban :
Pembahasan :
Diketahui :
Vef =120 V
Ief =12 A
ω =125 rad /s
R = 8 W
L = 32 mH
C = 800 mF
Ditanya : V = ……?
Untuk lebih jelasnya, silahkan lihat dan tontonlah Video YouTube di bawah ini :
GELOMBANG ELEKTOMAGNETIK
Sumber Materi : Quipper (Blog) dan Ruangguru (Blog)
[KETERANGAN : Untuk membaca Materi Fisika sebelumnya tentang Medan Magnet dan Induksi Elektromagnetik, silahkan baca dan lihat di sini.]
1. Pengertian Gelombang Elektromagnetik
Gelombang Elektromagnetik adalah Gelombang yang tidak membutuhkan medium untuk merambat. Artinya, Gelombang Elektromagnetik bisa merambat meskipun dalam ruang hampa seperti di luar angkasa.
Gelombang Elektromagnetik dibentuk oleh Medan Magnet dan Medan Listrik yang saling merambat tegak lurus. Sumber penghasil gelombang elektromagnetik berbeda-beda. Beberapa di antaranya dihasilkan oleh Nuklir atau Atomik yang di dalamnya memuat fisika kuantum. Perhatikan Ilustrasi Gelombang Elektromagnetik berikut ini.
Untuk Kelajuan Gelombang Elektromagnetik bisa ditentukan dengan persamaan berikut.
Keterangan :
c = Kelajuan Gelombang Elektromagnetik (m/s);
E = Besar Medan Listrik (N/C);
B = Besar Medan Magnet (T).
Dan berikut, inilah Sifat-sifat Gelombang Elektromagnetik.
 |
| Sumber : Blog Ruangguru |
2. Spektrum Gelombang Elektromagnetik
Spektrum Gelombang Elektromagnetik dengan urutan dari panjang gelombang terbesar atau Frekuensi terkecil ke panjang gelombang terkecil atau frekuensi terbesar sebagai berikut :
1. Gelombang Radio
Gelombang Radio merupakan Spektrum Gelombang Elektromagnetik yang memiliki panjang Gelombang terbesar dan Frekuensi terkecil. Gelombang ini dihasilkan oleh elektron pada kawat penghantar. Elektron tersebut nantinya akan menghasilkan arus bolak-balik pada kawat. Gelombang radio dipancarkan melalui Transmitter (Antena Pemancar) dan diterima oleh Receiver (Antena Penerima).
2. Gelombang Mikro
Gelombang Mikro merupakan Spektrum Gelombang Elektromagnetik yang memiliki frekuensi terkecil kedua setelah Gelombang Radio. Frekuensi Gelombang Mikro adalah 1010 Hz dengan panjang gelombang 3 mm. gelombang mikro biasa dimanfaatkan untuk kepentingan deteksi bawah laut menggunakan radar, membantu pendaratan pesawat, dan sebagainya.
3. Sinar Inframerah
Sinar Inframerah memiliki Frekuensi lebih besar daripada gelombang mikro. Frekuensi sinar inframerah berada di rentang 1011 Hz – 1014 Hz. Artinya, panjang gelombang sinar inframerah lebih kecil daripada gelombang radio dan gelombang mikro.
Sinar Inframerah banyak diaplikasikan dalam kehidupan sehari-hari, misalnya di bidang kedokteran untuk Terapi Saraf dan Penyembuhan Penyakit Encok, di bidang militer untuk melihat di tempat gelap atau berkabut, di bidang elektronika untuk remote control, dan masih banyak lainnya.
4. Cahaya Tampak
Jika di spektrum sebelumnya kamu tidak bisa melihat wujud gelombangnya, tidak demikian dengan cahaya tampak. Warna-warna Merah, Jingga, Kuning, Hijau, Biru, Nila, dan Ungu merupakan bentuk spektrum cahaya tampak. Cahaya tampak memiliki frekuensi sekitar 1015 Hz dengan panjang gelombang 400 nm – 800 nm.
Panjang gelombang terpendek dari cahaya tampak dimiliki oleh cahaya ungu. Artinya, cahaya ungu memiliki frekuensi dan energi terbesar dibandingkan warna lainnya. Sementara itu, panjang gelombang terpanjang dimiliki oleh cahaya merah. Aplikasi cahaya tampak bisa kamu lihat pada laser.
5. Sinar Ultraviolet
Sinar Ultraviolet atau biasa disingkat sinar UV merupakan spektrum gelombang elektromagnetik yang memiliki frekuensi 1015 – 1016 Hz. Panjang gelombang sinar UV adalah 10 – 100 nm. Sinar UV dihasilkan oleh radiasi sinar Matahari.
6. Sinar X
Sinar X merupakan spektrum Gelombang Elektromagnetik dengan frekuensi atau energi terbesar kedua setelah Sinar Gamma. Frekuensi sinar X berada di kisaran 1016 – 1020 Hz. Sinar ini ditemukan oleh Wilhelm Rontgen. Itulah mengapa sinar X juga biasa disebut sinar Rontgen. Sinar X dihasilkan oleh aktivitas elektron berkecepatan tinggi yang menumbuk logam. Tumbukan antara Elektron dan logam disertai pelepasan energi dalam bentuk radiasi sinar X. Oleh karena energinya sangat besar, tak heran jika sinar X mampu menembus logam dan tulang manusia.
7. Sinar Gamma
Sinar Gamma merupakan spektrum gelombang elektromagnetik dengan energi tertinggi. Hal itu dikarenakan sinar gamma memiliki frekuensi tertinggi di antara spektrum gelombang elektromagnetik lainnya, yaitu 1020 – 1025 Hz. Mengingat energi sinar gamma sangat besar, tak heran jika sinar ini bisa menembus logam beberapa sentimeter. Sinar gamma dihasilkan oleh aktivitas radioaktif atau atom-atom yang tidak stabil di reaksi inti.
Dan inilah Ilustrasi Konsep Gelombang Elektromagnetik yang ada di bawah ini.
Untuk Rentang Frekuensinya, bisa kalian lihat di Bagan berikut.
3. Sifat-Sifat Gelombang Elektromagnetik
Adapun Sifat-sifat Gelombang Elektromagnetik adalah sebagai berikut.
1. Memiliki kecepatan konstan di ruang hampa, yaitu sebesar 3 × 108 m/s.
2 Tidak dipengaruhi oleh medan listrik maupun medan magnet karena tidak bermuatan listrik.
3. Termasuk Gelombang Transversal.
4. Energinya bergantung pada besarnya frekuensi. Hal itu didasarkan pada persamaan Planck berikut.
Keterangan :
E = Energi Radiasi (J);
h = Konstanta Planck = 6,6 × 1034 Js;
f = Frekuensi (Hz);
c = Kelajuan Cahaya = 3 × 108 m/s;
λ = Panjang Gelombang
(m).
3. Manfaat Gelombang Elektromagnetik
Gelombang elektromagnetik memiliki manfaat yang sangat besar dalam kehidupan. Inilah manfaat Gelombang Elektromagnetik.
1. Gelombang Radio
Gelombang yang digunakan sebagai gelombang pembawa Audio (Suara). Biasanya kamu kenal sebagai Radio.
2. Gelombang Mikro
Adapun manfaat Gelombang Mikro adalah sebagai berikut.
- Pemanas Makanan (Microwave).
- Untuk komunikasi pada Teknologi RADAR.
- Menganalisis Struktur Atomik dan Molekul.
- Memandu pendaratan Pesawat.
- Mendeteksi keberadaan suatu objek.
3. Sinar Inframerah
Adapun manfaat Sinar Inframerah adalah sebagai berikut.
- Untuk Terapi Fisik, misalnya menyembuhkan penyakit cacar dan encok.
- Untuk fotografi pemetaan Sumber Daya Alam (SDA).
- Digunakan pada Remote Control.
- Mengeringkan Cat kendaraan dengan cepat pada Industri Otomotif.
4. Cahaya Tampak
Untuk cahaya tampak, memiliki manfaat berikut ini.
- Sinar laser digunakan pada bidang telekomunikasi untuk menyalurkan suara, gambar, atau sinyal melalui serat optik.
- Sinar laser digunakan di bidang kedokteran sebagai alat untuk mendiagnosis penyakit.
- Di bidang industri, sinar laser digunakan untuk mengelas dan memotong lempengan baja.
5. Sinar Ultraviolet
Sinar ultraviolet bisa dimanfaatkan untuk hal-hal berikut.
- Proses fotosintesis atau asimilasi pada tumbuhan.
- Pembentukan vitamin D.
- Membunuh kuman penyakit.
- Mensterilkan ruangan.
- Memeriksa keaslian tanda tangan di dunia perbankan.
6. Sinar X
Sinar X bisa dimanfaatkan untuk hal-hal berikut.
- Memotret organ-organ dalam tubuh seperti tulang, jantung, dan paru-paru.
- Menganalisis struktur bahan atau kristal.
- Mendeteksi keretakan atau cacat pada logam.
- Memeriksa barang-barang di bandara.
7. Sinar Gamma
Sinar Gamma bermanfaat untuk hal-hal berikut.
- Terapi Kanker.
- Sterilisasi peralatan rumah sakit.
- Sterilisasi makanan kemasan.
- Pembuatan varietas tanaman unggul tahan hama.
- Mengurangi populasi hama.
TEORI RELATIVITAS KHUSUS
Sumber Materi : Quipper (Blog) dan Studiobelajar.com
Sir Isaac Newton menganggap ruang dan waktu itu konstan, akan tetapi pada sebuah pemahaman baru yang diberikan oleh teori relativitas umum dan teori relativitas khusus, ruang dan waktu tidaklah konstan, melainkan dapat berubah dan bergejolak layaknya fluida.
Albert Einstein merupakan ilmuwan dibalik teori ini dimana dia mempublikasikan bagian pertama teori ini yakni teori relativitas khusus pada tahun 1905. Satu dekade kemudian, Einstein mempublikasikan bagian keduanya yakni teori relativitas umum.
A. Teori Relativitas Khusus
Inilah beberapa Teori Relativitas Khusus didasarkan pada dua postulat Einstein, yaitu sebagai berikut :
- Hukum Fisika dapat dinyatakan dalam bentuk matematis yang sama, meskipun diamati dari kerangka acuan yang bergerak dengan kecepatan tetap terhadap kerangka acuan yang lain.
- Kelajuan cahaya dalam ruang hampa adalah konstan untuk semua pengamat, tidak bergantung pada gerak sumber cahaya maupun pengamat.
1. Relativitas Kecepatan
Tidak ada kecepatan yang melebihi kecepatan cahaya. Rumus penjumlahan kecepatan relativitas ialah sebagai berikut.
2. Relativitas Panjang
Menurut teori ini, jika benda bergerak mendekati kecepatan cahaya, maka panjang benda seolah-olah tampak memendek (kontraksi panjang). Apabila diukur oleh pengamat yang diam terhadap benda tersebut, relativitas panjang bisa dirumuskan sebagai berikut :
3. Relativitas Massa
Jadi, kalau kata Einstein, massa benda yang bergerak (m) akan lebih besar daripada massa benda tersebut saat diam (mo). Rumusnya adalah sebagai berikut :
4. Relativitas Waktu (Dilatasi Waktu)
Merupakan waktu yang diukur oleh sebuah jam yang bergerak terhadap kejadian lebih besar daripada jam yang diam terhadap kejadian. Relativitas waktu bisa dirumuskan sebagai berikut :
5. Kesetaraan Massa dan Energi
Menurut Einstein, jika terjadi penyusutan massa, maka akan timbul energi. Hal ini menunjukkan adanya kesetaraan massa dan energi. Benda yang diam maupun bergerak memiliki energi.
Energi saat benda diam dan saat bergerak atau Energi Total dapat dirumuskan sebagai berikut.
6. Momentum Relativistik
Tiap benda yang bergerak dengan kecepatan v, memiliki momentum linier yang berbanding lurus dengan massa dan kecepatannya. Momentum suatu benda bergerak dengan kecepatan mendekati kecepatan Cahaya c, akan mengalami perubahan dalam momentum tersebut karena mengalami Gejala Relativitas. Berikut ini rumusnya.
B. Fenomena Kuantum
Inilah beberapa tokoh fenomena kuantum di alam adalah Arthur Compton, C. V. Raman, dan Pieter Zeeman. Masing-masing tokoh ini punya nama efek kuantum dari namanya sendiri.
1. Teori Max Planck
Teori kuantum dikemukakan oleh Plank terkait dengan cahaya. Cahaya merupakan gelombang elektromagnetik berupa paket-paket energi yang terkuantisasi (diskrit) yang tak bermuatan dan disebut dengan “Foton”. Energi satu foton dirumuskan sebagai berikut.
2. Efek Fotolistrik
Nah, kalau Efek Fotolistrik ialah gejala terlepasnya elektron dari permukaan logam saat dijatuhi gelombang elektromagnetik. Menurut Einstein, Elektron-elektron pada permukaan gelombang menyerap energi gelombang elektromagnetik yang memiliki energi ikat sebesar h⋅f⋅o dan elektron yang keluar berenergi Ek= 1/2⋅mv2. Syarat Elektron keluar dari permukaan logam adalah sebagai berikut.
Sementara energi kinetik elektron dan potensial henti dirumuskan sebagai berikut.
3. Efek Compton
Pada percobaan penembakan elektron yang diam oleh foton, ternyata elektron tersebut terpental. Fotonnya terhambur dengan energi lebih kecil karena panjang gelombangnya lebih besar daripada foton yang datang. Pergeseran panjang gelombang foton dirumuskan sebagai berikut.
4. Difraksi Elektron
Menurut teori fisika klasik, elektron punya perilaku seperti partikel. Elektron hanya berpindah pada garis lurus dan tidak membelok, kecuali terdapat faktor luar seperti medan magnet.
Hasil eksperimen Davisson-Germer menunjukkan bahwa elektron memiliki sifat gelombang. Elektron akan terdifraksi melalui celah sangat sempit dan saling berinteraksi seperti gelombang. Hal ini bersesuaian dengan hipotesis de Broglie, di mana elektron memiliki dualisme sifat gelombang-partikel.
5. Radiasi Benda Hitam
Ayo, siapa yang belum tahu tentang benda hitam? Benda hitam adalah benda yang akan menyerap seluruh radiasi yang mengenainya atau benda yang tidak memantulkan cahaya yang mengenainya. Radiasi yang dipancarkan benda hitam disebut dengan radiasi benda hitam.
Berdasarkan Hukum Stefan-Boltzmann, “Jumlah energi yang dipancarkan benda hitam per satuan luas permukaan per satuan waktu akan berbanding lurus dengan pangkat empat temperatur termodinamikanya”. Rumusnya dapat dinyatakan sebagai berikut.
6. Hukum Pergeseran Wien
Hukum pergeseran Wien menjelaskan bahwa spektrum radiasi benda hitam pada suhu berapa pun berkorelasi dengan spektrum pada suhu lainnya. Dengan kata lain, jika bentuk spektrum pada suatu suhu diketahui, bentuk spektrum pada suhu lainnya dapat ditentukan. Menurut Wien, “Panjang gelombang untuk intensitas cahaya maksimum berkurang dengan meningkatnya suhu”. Berikut rumusnya.
7. Panjang Gelombang de Broglie
Pada Tahun 1924, seorang Fisikawan asal Prancis, Louis de Broglie menyatakan hipotesisnya tentang dualisme gelombang-partikel. Menurut de Broglie, semua partikel juga memiliki sifat seperti gelombang. Panjang gelombang de Broglie untuk partikel dirumuskan sebagai berikut.
Untuk lebih jelasnya, silahkan lihat dan tontonlah Video YouTube di bawah ini :
SUMBER ENERGI
Sumber Materi : Pakdosen.co.id dan Dosenpendidikan.co.id
A. Pengertian Sumber Energi
Sumber Energi adalah sumber daya yang dapat diolah oleh manusia sehingga dapat digunakan bagi pemenuhan kebutuhan energi. Sumber energi ini disebut sumber energi primer, yaitu sumber daya energi dalam bentuk apa adanya yang tersedia di alam.
|
Tabel 1
Cadangan Energi Primer Dunia. |
||
|
cadangan
Minyak Bumi |
Indonesia :
1,1 % |
Timur Tengah
: 70 % |
|
Cadangan Gas
Bumi |
Indonesia :
1-2 % |
Rusia :
25 % |
|
Cadangan
Batubara |
Indonesia :
3,1 % |
Amerika
Utara : 25 % |
Penyediaan Energi di Indonesia
Mengingat akan banyaknya kebutuhan energi yang diperlukan untuk menggerakkan pembangunan khususnya dalam bidang Industri seperti telah ditampilkan pada Grafik l di atas, maka persoalan berikutnya adalah bagaimana mengenai penyediaan energi untuk memenuhi kebutuhan energi tersebut. Mengenai penyediaan energi tersebut usaha diversifikasi telah dilakukan agar kebutuhan energi tidak semata-mata tergantung pada minyak bumi saja.
Bila dikaji dari data yang telah diolah, tampak bahwa usaha diversifikasi Energi Primer telah berhasil menurunkan pangsa pemakaian minyak bumi dalam usaha memenuhi kebutuhan energi dari 63,7 % pada akhir Pelita V menjadi 52,3 % pada akhir Pelita Vl. Sedangkan pangsa pemakaian batubara mengalami kenaikan dari 8,2 % pada akhir Pelita V menjadi 17,5 % pada Tahun 1998 - 1999 ini.
Selain dari pada itu, bila dikaji lebih cermat ternyata pemakaian Energi Panas Bumi yang selama ini sering terabaikan, ternyata sudah mulai diperhatikan sebagai usaha mencukupi kebutuhan energi di Indonesia. Hal ini tampak dari kenyataan bahwa pada tahun 1994/95 (akhir Pelita V) pangsa energi panas bumi hampir tak berarti hanya sekitar 0,6 % saja dari seluruh pemenuhan kelzutuhan energi, akan tetapi pada tahun 1998/99 pangsa energi panas bumi telah naik hampir 3 kali lipat menjadi 1,7 %. Keadaan ini sudah barang tentu sangat memberikan harapan bagi pengembangan energi panas bumi pada masa mendatang.
Oleh karena itu kita harus pandai-pandai untuk menghemat energi. Bukan hanya energi listrik beberapa pekan yang lalu kita dengar adanya pemadaman listrik disejumlah daerah, tetapi juga energi yang lain seperti Minyak Goreng. Di berita saat ini sedang marak dibicarakan tentang kenaikan minyak goreng ataupun kelangkaan minyak goreng di beberapa daerah. Padahal kita tahu Indonesia termasuk salah satu anggota OPEC. OPEC adalah organisasi bagi negara-negara pertambangan minyak. Dan saat ini terancam dikeluarkan dari OPEC
B. Macam-macam Sumber Energi
Sumber Energi terbagi menjadi 2 (Dua) Macam yaitu sumber Energi Non-konvesional dan sumber Energi Konvesional, dibawah ini adalah penjelasannya yaitu sebagai berikut :
1. Sumber Energi Nonkonvensional
Beberapa alternatif pengembangan sumber energi nonkonvensional yang dikembangkan untuk mengganti sumber energi konvensional yang terbatas jumlahnya adalah sebagai berikut :
a. Energi Matahari
Cahaya Matahari dapat diubah menjadi Energi Listrik dengan jalan menangkap cahaya matahari dengan beribu-ribu Fotosel. Fotosel dapat dibuat dari Silikon yang sisi-sisinya dilapisi dengan Boron dan Arsen. Untuk mendapatkan Voltase yang tinggi dan arus yang kuat, Ribuan Fotosel dihubungkan secara seri-paralel. Energi matahari dapat juga diubah menjadi energi panas dengan pertolongan Cermin Cekung.
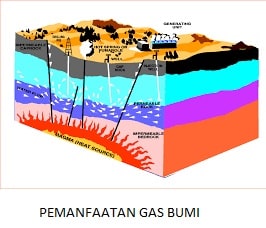
b. Energi Panas Bumi
Panas dari Gunung Berapi bersumber dari Magma. Bila di dekat magma tersebut terdapat cadangan air maka air itu akan mendapatkan panas. Rembesan air panas ke permukaan bumi dapat merupakan sumber air panas, berupa semburan uap atau semburan air panas. Panas bumi berupa uap air panas dapat digunakan untuk menggerakkan turbin yang dapat menggerakkan Generator Listrik.
c. Energi Angin
Langsung dapat diubah menjadi listrik dengan menggunakan kincir angin yang dihubungkan dengan generator listrik.
d. Energi Pasang Surut
Dapat dimanfaatkan dengan menggunakan dam yang memiliki pintu air yang dapat diatur pembukaannya. Pada saat air laut pasang, air laut masuk ke dalam dam melalui pintu air. Bila air surut maka air laut akan ke luar juga melalui pintu air yang sama. Di pintu air itulah dipasang turbin yang dapat menggerakkan generator listrik.
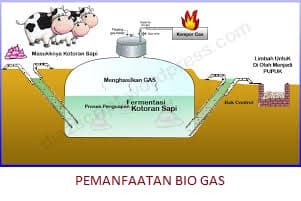
e. Energi Biogas
Prinsipnya adalah memanfaatkan jasad hidup sampah melalui cara pembusukan dengan pertolongan bakteri pengurai. Bakteri itu diperoleh dari Kotoran Kerbau atau Sapi. Gas yang sebagian besar adalah metan dapat dibakar untuk keperluan masak memasak.
f. Energi Biomassa
Bahan bakunya adalah sampah organik. Panas yang timbul, digunakan untuk memanaskan ketel uap. Uap yang dihasilkan digunakan untuk menggerakkan generator listrik.
2. Sumber Energi Konvensional
Sumber Daya Energi Konvensional adalah sumber daya energi yang digunakan untuk memenuhi sebagian besar kebutuhan energi manusia sekarang. Sumber daya energi konvensional terdiri dari :
- Minyak bumi
- Batubara
- Gas alam
C. Jenis-Jenis Sumber Energi
Energi adalah ukuran dari kesanggupan benda tersebut untuk melakukan suatu usaha. Energi berasal dari Bahasa Yunani yaitu energia yang berarti kemampuan untuk melakukan usaha. Energi merupakan besaran yang kekal, artinya energi tidak dapat diciptakan dan dimusnahkan, tetapi dapat diubah dari suatu bentuk satu ke bentuk yang lain namun tidak merubah jumlah atau besar Energi secara keseluruhan.
Dalam pengertian sehari-hari energi merupakan kemampuan untuk melakukan gerak, jika suatu objek mampu untuk melakukan gerakan, maka obyek tersebut dikatakan mempunyai Energi. Menurut ilmu Fisika, terdapat berbagai macam bentuk energi diantaranya :
1. Energi Kinetik
Energi Kinetik adalah energi dari suatu benda yang dimiliki karena pengaruh gerakannya, contohnya ketika seseorang yang sedang berlari, maka posisi orang tersebut akan berubah setiap detiknya, perubahan posisi ini menunjukkan bahwa orang itu memiliki energi.
2. Energi Potensial
Energi Potensial adalah Energi yang dimiliki suatu benda akibat adanya pengaruh tempat atau kedudukan dari benda tersebut. Energi Potensial disebut juga dengan energi diam karena benda yang dalam keaadaan diam dapat memiliki energi. Jika benda tersebut bergerak, maka benda itu mengalami perubahan Energi Potensial menjadi energi gerak. Energi potensial memiliki beberapa bentuk diantaranya : Energi Potensial Gravitasi, Energi Potensial Pegas, dan lain-lain.
3. Energi Panas
Energi Panas adalah energi ini muncul saat terjadinya perubahan suhu benda, dan menjalar dari bagian yang panas ke bagian yang dingin. Energi ini dapat dideteksi dengan indera peraba dan Thermometer.
4. Energi Kimia
Energi Kimia adalah energi yang tersimpan secara kimiawi. Misalnya makanan yang kita makan menghasilkan energi kimia yang sangat bermanfaat bagi tubuh. Minyak bumi mengandung energi kimia yang sangat bermanfaat untuk bahan bakar. Baik energi kimia dalam makanan maupun energi kimia dalam minyak bumi berasal dari energi matahari.
5. Energi Nuklir
Energi Nuklir adalah energi yang tersimpan dalam atom. Energi keluar ketika terjadi proses reaksi nuklir. Energi ini diperoleh dari hasil reaksi inti, yaitu reaksi yang terjadi pada inti atom dimana partikel – partikel berenergi tinggi bertumbukkan dengan inti atom tersebut sehingga terbentuklah inti baru yang berbeda dengan inti semula.
6. Energi Listrik
Energi Listrik adalah energi yang ditimbulkan oleh benda yang bermuatan listrik. Muatan listrik yang diam (Statis) menimbulkan energi potensial listrik, sedangkan muatan listrik yang bergerak (Dinamis) menimbulkan Arus Listrik dan Energi Magnet.
D. Perubahan Energi
Ketika sebuah batu jatuh dari suatu ketinggian, batu tersebut memiliki Energi. Jika batu tersebut jatuh ke tanah, Energi ini akan diubah menjadi Energi panas (dapat teramati pada tanah yang menjadi hangat ketika terkena batu) dan Energi Bunyi. Jadi, Energi tidak pernah hilang, tetapi diubah kedalam bentuk Energi lain.
Dengan konsep di atas, maka Energi dapat dimanfaatkan dalam kehidupan sehari-hari. Contoh perubahan Energi antara lain sebagai berikut :
- Energi Listrik menjadi Energi Cahaya, misalnya pada Lampu
- Energi Listrik menjadi Energi Kimia, misalnya pada Pengisian Aki, Pengisian Baterai Isi Ulang.
- Energi Cahaya menjadi Energi Kimia, misalnya Fotosintesis
- Energi Listrik menjadi Energi bunyi, misalnya Bel Listrik, Radio, Tape Recorder, dan Televisi (TV).
- Energi Listrik menjadi Energi Gerak, misalnya Kipas Angin, Blender, Mikser (Mixer) dll.
- Energi Listrik menjadi Energi Panas, misalnya Setrika Listrik, Solder Listrik, Kompor Listrik, Magic Jar, Pemanggang Listrik
- Energi Listrik menjadi Energi Magnet, misaknya Alat Pengangkat Besi yang menggunakan Magnet Listrik
- Energi Kimia menjadi Energi Listrik, misalnya Baterai dan aki pada saat digunakan
- Energy Kimia menjadi Energi Gerak, misalnya Makanan yang kita makan dapat menghasilkan Energi sehingga kita dapat bergerak dan melakukan aktivitas
- Energi Kimia menjadi Panas, misalnya Minyak Tanah yang digunakan untuk menyalakan Kompor menghasilkan Panas
- Energi Kinetik menjadi Energi Bunyi, misalnya Benda yang jatuh dari ketinggian tertentu akan menghasilkan Bunyi
- Energi Gerak menjadi Energi Panas, misalnya Roda-roda Mesin yang saling bergesekan dapat menghsilkan Panas
- Energi Kinetik menjadi Energi Listrik, misalnya Dinamo yang diputar atau digerakkan oleh Ban Sepeda
E. Pemanfaatan Energi
Berikut ini adalah contoh-contoh Pemanfaatan Energi dalam kehidupan sehari-hari :
- Pesawat memanfaatkan tenaga dari putaran baling-baling
- Sel surya memanfaatkan Energi Cahaya Matahari
- Perahu layar memanfaatkan Energi Angin
- Terompet memanfaatkan Energi dari Tiupan
- Kincir angin memanfaatkan Energi Angin
- Kincir air memanfaatkan Energi Air
- Dinamo sepeda memanfaatkan Energi Gerak
- PLTN memanfaatkan Energi Nuklir
- PLTU memanfaatkan Energi Uap
STRUKTUR ATOM
Sumber Materi : Quipper (Blog)
1. Asal usul Teori Atom
Kata Atom berasal dari Bahasa Yunani yaitu ”atomos” yang berarti ”tidak dapat dibagi”. Konsep dasar atom pertama kali dikemukakan oleh Democritus (orang Yunani) pada awal abad ke-4 Sebelum Masehi.
Menurut teori yang dikemukakannya, suatu benda dapat dibagi menjadi bagian-bagian yang sangat kecil yang akhirnya tidak dapat dibagi lagi yang disebut atom. Menurut Democritus atom sepenuhnya padat, tidak memiliki struktur internal, serta ada ruang kosong antar atom untuk memberikan ruang untuk pergerakannya (seperti pergerakan dalam air dan udara, atau fleksibilitas benda padat).
Selain itu, Democritus juga menjelaskan bahwa untuk menjelaskan perbedaan sifat dari material yang berbeda, atom dibedakan ke dalam bentuk, massa dan ukurannya. Berdasarkan model atom yang dibuatnya, Democritus mampu menjelaskan bahwa semua benda terdiri dari bagian yang lebih kecil disebut atom. Namun model Democritus ini kurang memiliki bukti Eksperimental hingga mulai Tahun 1800an muncul teori-teori baru berdasarkan hasil eksperimen.
Beberapa teori yang menjelaskan tentang atom adalah sebagai berikut :
2. Model Teori Atom John Dalton
John Dalton pada Tahun 1803 mengemukakan pendapatnaya tentang atom. Teori atom Dalton didasarkan pada dua hukum, yaitu hukum kekekalan massa (Hukum Lavoisier) dan hukum susunan tetap (Hukum Prouts). Lavosier mennyatakan bahwa “Massa total zat-zat sebelum reaksi akan selalu sama dengan massa total zat-zat hasil reaksi.” Sedangkan Prouts menyatakan bahwa “Perbandingan massa unsur-unsur dalam suatu senyawa selalu tetap.”
Dari kedua Hukum tersebut Dalton mengemukakan pendapatnya tentang atom sebagai berikut :
- Atom merupakan bagian terkecil dari materi yang sudah tidak dapat dibagi lagi.
- Atom digambarkan sebagai bola pejal yang sangat kecil, suatu unsur memiliki atom-atom yang identik dan berbeda untuk unsur yang berbeda.
- Atom-atom bergabung membentuk senyawa dengan perbandingan bilangan bulat dan sederhana. Misalnya air terdiri atom-atom hidrogen dan atom-atom oksigen.
- Reaksi kimia merupakan pemisahan atau penggabungan atau penyusunan kembali dari atom-atom, sehingga atom tidak dapat diciptakan atau dimusnahkan.
Kelebihan :
Mulai membangkitkan minat terhadap penelitian mengenai model atom.
Kelemahan :
Teori atom Dalton tidak dapat menerangkan suatu larutan dapat menghantarkan arus listrik. Bagaimana mungkin bola pejal dapat menghantarkan arus listrik? padahal listrik adalah elektron yang bergerak. Berarti ada partikel lain yang dapat menghantarkan arus listrik.
3. Model Teori Atom JJ. Thomson
J.J. Thomson pada awal Tahun 1900an, mengemukakan teori baru tentang atom. Menurutnya di dalam atom terdapat partikel elektron dan proton. Berdasarkan hasil eksperimennya, proton memiliki massa yang jauh lebih besar dibandingkan elektron, sehingga model atom Thomson menggambarkan atom sebagai proton tunggal yang besar.
Di dalam Proton terdapat Elektron-elektron yang menetralkan adanya muatan positif dari proton. Menurut Thomson, atom terdiri dari suatu bulatan bermuatan positif dengan rapat muatan yang merata. Di dalam muatan positif ini tersebar elektron dengan muatan negatif yang besarnya sama dengan muatan positif. Secara garis besar teori atom thomson adalah “Atom merupakan bola pejal yang bermuatan positif dan didalamya tersebar muatan negatif elektron.”
Secara sederhana Model Atom Thomson dapat analogikan sebagai jambu biji yang telah dikelupas kulitnya. Biji jambu yang tersebar merata dimodelkan sebagai Elektron dan bulatan daging jambu yang pejal dimodelkan sebagai Proton.
Kelebihan :
Membuktikan adanya partikel lain yang bermuatan negatif dalam atom. Berarti atom bukan merupakan bagian terkecil dari suatu unsur.
Kelemahan :
Model Thomson ini tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom tersebut.
4. Model Atom Rutherford
Pada Tahun 1910 Rutherford bersama 2 Orang muridnya (Hans Geiger dan Erners Masreden) melakukan percobaan yang dikenal dengan hamburan Sinar Alfa (λ) terhadap Lempeng Tipis Emas. Dari hasil pengamatannya ditemukan bahwa sebagian besar partikel alfa mampu menembus lembaran Emas tanpa dibelokkan.
Bersamaan dengan itu, Rutherford juga menemukan partikel alfa yang dibelokkan sedikit, namun dengan sangat mengejutkan, Rutherford juga menemukan beberapa partikel alfa yang dibelokkan pada sudut yang sangat tajam kembali ke sumber radioaktif. Untuk menjelaskan adanya sebagian besar partikel-α yang menembus Lempeng Emas tanpa dibelokkan, Rutherford kemudian mengembangkan model Inti Atom.
Berdasarkan gejala-gejala yang terjadi, Rutherford membuat kesimpulan bahwa :
- Atom bukan merupakan Bola Pejal, karena hampir semua partikel alfa diteruskan
- Jika Lempeng Emas tersebut dianggap sebagai satu lapisanatom-atom Emas, maka di dalam atom emas terdapat partikel yang sangat kecil yang bermuatan positif.
- Partikel tersebut merupakan partikelyang menyusun suatu inti atom, berdasarkan fakta bahwa 1 dari 20.000 Partikel Alfa akan dibelokkan. Bila perbandingan 1:20.000 merupakan perbandingan diameter, maka didapatkan ukuran inti atom kira-kira 10.000 lebih kecil daripada ukuran atom keseluruhan.
Berdasarkan kesimpulan dari hasil pengamatannya Rutherford mengemukan sebuah model atom yang dikenal dengan model atom Ruthreford yaitu ” Atom terdiri dari inti atom yang sangat kecil dan bermuatan positif, dikelilingi oleh elektron yang bermuatan negatif.”
Kelebihan :
Membuat hipotesis bahwa atom tersusun dari inti atom dan elektron yang mengelilingi inti. Teori Rutherford bahwa elektron mengelilingi inti atom ini memberikan inspirasi pada penemuan baru berikutnya yaitu tentang lintasan/kedudukan elektron yang selanjutnya dikenal sebagai kulit elektron.
Kelemahan :
Tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom. Berdasarkan teori gerak, apabila Elektron bergerak mengitari inti disertai pemancaran energi maka lama – kelamaan Energi Elektron akan berkurang dan lintasannya makin lama akan mendekati inti dan jatuh ke dalam Inti.
5. Model Atom Niels Bohr
Pada Tahun 1913, Neils Bohr memperbaiki kegagalan Atom Rutherford melalui percobaannya tentang spektrum atom hidrogen. Berdasarkan hasil percobaannya Bohr memberikan gambaran keadaan/kedudukan orbit elektron dalam menempati daerah di sekitar inti atom. Menurut Bohr elektron mengelilingi inti atom pada orbit tertentu, hanya terdapat orbit dalam jumlah tertentu dan perbedaan antar orbit satu dengan yang lain adalah jarak orbit dari inti atom.
Keberadaan elektron baik di orbit yang rendah maupun yang tinggi sepenuhnya tergantung oleh tingkatan energi elektron. Sehingga Elektron di orbit yang rendah akan memiliki energi yang lebih kecil daripada elektron di orbit yang lebih tinggi.
Penjelasan Bohr tentang atom melibatkan gabungan antara teori klasik dari Rutherford dan teori kuantum dari Planck, dan secara garis besar Bohr mengemukaan model atomnya sebagai berikut :
- Elektron dalam atom bergerak mengelilingi inti pada lintasan-lintasan tertentu, tidak memancarkan energi. Lintasan-lintasan elektron itu disebut kulit atau tingkat energi elektron.
- Elektron dapat berpindah dari satu lintasan ke lintasan yang lain.
- Perpindahan elektron dari tingkat energi tinggi ke rendah disertai pemancaran energi. Sedang perpindahan elektron dari tingkat energi rendah ke tinggi disertai penyerapan energi.
- Elektron yang bergerak pada lintasannya berada pada keadaan stasioner, artinya elektron tidak memancarkan atau menyerap energi.
Menurut Model Atom Bohr, elektron-elektron mengelilingi inti pada lintasan-lintasan tertentu yang disebut kulit elektron atau tingkat energi. Tingkat energi paling rendah adalah kulit elektron yang terletak paling dalam, semakin keluar semakin besar nomor kulitnya dan semakin tinggi tingkat energinya.
Kelebihan :
Atom Bohr adalah bahwa Atom terdiri dari beberapa kulit untuk tempat berpindahnya Elektron.
Kelemahan :
Model Atom ini adalah tidak dapat menjelaskan Efek Zeeman dan Efek Strack.
6. Model Atom Modern
Berdasarkan pengertian dasar yang diperoleh dari model-model atom klasik bahwa atom terdiri dari elektron, proton, dan neutron, maka dapat dimungkinkan adanya model yang lebih rumit dan lengkap mengenai atom yang hingga sekarang masih dikatakan misterius.
Salah seorang yang menjelaskan tentang model atom modern adalah Erwin Schrodinger (1926). Sebelum Erwin Schrodinger, seorang ahli dari Jerman Werner Heisenberg mengembangkan teori mekanika kuantum yang dikenal dengan prinsip ketidakpastian yaitu “Tidak mungkin dapat ditentukan kedudukan dan momentum suatu benda secara seksama pada saat bersamaan, yang dapat ditentukan adalah kebolehjadian menemukan elektron pada jarak tertentu dari inti atom.”
Daerah ruang di sekitar inti dengan kebolehjadian untuk mendapatkan elektron disebut orbital. Bentuk dan tingkat energi orbital dirumuskan oleh Erwin Schrodinger.Erwin Schrodinger memecahkan suatu persamaan untuk mendapatkan fungsi gelombang untuk menggambarkan batas kemungkinan ditemukannya Elektron dalam Tiga Dimensi (3D).
x,y dan z = Posisi dalam tiga dimensi
y= Fungsi gelombang
m= massa
ђ= h/2p dimana h = konstanta plank dan p = 3,14
e= Energi total
V= Energi potensial
Model Atom dengan orbital lintasan elektron ini disebut model atom modern atau model atom mekanika kuantum yang berlaku sampai saat ini, seperti terlihat pada gambar berikut ini.
Awan Elektron di sekitar inti menunjukan tempat kebolehjadian elektron. Orbital menggambarkan tingkat energi elektron. Orbital-orbital dengan tingkat energi yang sama atau hampir sama akan membentuk sub kulit. Beberapa sub kulit bergabung membentuk kulit. Dengan demikian kulit terdiri dari beberapa sub kulit dan subkulit terdiri dari beberapa orbital.
Demikianlah semoga membantu khususnya untuk menyelesaikan soal Ujian Akhir Tahun (PAT) Mata Pelajaran Fisika Kelas 12.
Mohon maaf apabila ada sedikit Kesalahan, baik itu Salah Kata, ataupun Salah menulis Rumus.Terima Kasih 😀👍 :)
Wassalammu‘alaikum wr. wb.






































.png)
No comments:
Post a Comment